Januskinase-Inhibitoren (JAKi) – wie ist mit den Verordnungseinschränkungen umzugehen?
Aktualisierte Empfehlungen der Deutschen Gesellschaft für Rheumatologie und Klinische Immunologie
17.10.2024
Vorwort
Im November 2022 hat der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) Empfehlungen zur Verordnung von JAKi formuliert, um das Risiko von schwerwiegenden unerwünschten Arzneimittelwirkungen zu minimieren. Diese ganz überwiegend auf den Daten der ORAL SURVEILLANCE-Studie basierenden und sich auf das Risiko kardiovaskulärer Ereignisse und die Entstehung von Malignomen beziehenden Empfehlungen haben zu einer großen Verunsicherung im Umgang mit JAKi und Veränderungen im Verordnungsverhalten geführt. Inzwischen liegen zusätzliche Daten zur Arzneimittelsicherheit und Nebenwirkungsprofil von JAKi sowie zur besseren Einschätzung der das Nebenwirkungsrisiko ganz entscheidend beeinflussenden Risikofaktoren vor. Diese sind Grundlage dieser Aktualisierung der DGRh-Empfehlungen zum Umgang mit JAKi in der Rheumatologie.
Therapeutischer Stellenwert der JAK-Inhibitoren
Seit rund sieben Jahren sind JAK-Inhibitoren (JAKi) in Deutschland zur Behandlung rheumatischer Erkrankungen im Einsatz. Ihre Zulassung erfolgte für alle vier in Deutschland zur Verfügung stehenden JAKi (in der zeitlichen Reihenfolge Baricitinib, Tofacitinib, Upadacitinib, Filgotinib) zunächst zur Behandlung der rheumatoiden Arthritis (RA). Zwei der Substanzen, Tofacitinib und Upadacitinib, sind unterdessen auch bei der Arthritis psoriatica und der axialen Spondyloarthritis (Spondylitis ankylosans) zugelassen, Tofacitinib seit August 2021 auch bei Subtypen der juvenilen idiopathischen Arthritis. Vor allem bei der RA haben sich die JAKi aufgrund ihrer guten, einigen Biologika überlegenen Wirksamkeit einen festen Stellenwert erworben. Nach der letzten Auswertung aus der Kerndokumentation des Deutschen Rheumaforschungszentrums (DRFZ) standen 2022 etwa 11 % der RA-Patient:innen unter dieser Therapie, darunter rund zwei Drittel in Monotherapie (1). Zu den positiven Eigenschaften dieser Substanzgruppe zählen neben der oralen Verabreichung der schnelle Wirkeintritt, die gute Wirkung in Monotherapie und, aufgrund der kurzen Halbwertszeit, die gute Steuerbarkeit mit kurzer Ausschleichphase falls eine Therapiepause z.B. wegen unerwünschter Wirkungen oder geplanter operativer Eingriffe nötig ist. In einigen kontrollierten RA-Studien waren die JAKi in der Wirksamkeit Adalimumab (2,3,4) bzw. Abatacept (5) überlegen. In einer weiteren, investigator-initiierten holländischen Studie zeigte Baricitinib im Vergleich mit unterschiedlichen TNFi über 48 Wochen einen signifikant besseren Outcome (6). Neben den Einsatzbereichen in der Rheumatologie sind einige JAKi zudem auch in dermatologischen Indikationen und in der Therapie chronisch-entzündlicher Darmerkrankungen zugelassen.
Oral Surveillance-Studie
Bei ORAL-SURVEILLANCE (7), einer 2014 auf Anforderung der U.S. Food and Drug Administration (FDA) für den JAKi Tofacitinib initiierten Sicherheitsstudie, handelte es sich um einen randomisierten, offenen Vergleich (Ratio 1:1:1) zwischen Tofacitinib in der rheumatologischen Dosierung (2x5 mg täglich) und der doppelt so hohen Dosierung (2x10 mg) und den TNF-Inhibitoren (TNFi) Adalimumab und Etanercept. Eingeschlossen wurden Patientinnen und Patienten mit RA ab einem Alter von 50 Jahren, die zuvor nicht ausreichend auf Methotrexat (MTX) angesprochen hatten und mindestens einen kardiovaskulären Risikofaktor aufwiesen. Adalimumab in üblicher Dosierung wurde in USA, Puerto Rico und Kanada, Etanercept im Rest der Welt verwendet. Alle Substanzen wurden in Kombination mit MTX gegeben. Beteiligt waren 323 Zentren in 30 Ländern.
Es handelte sich um eine Endpunkt getriebene Studie, die erst bei Erreichen von mindestens 103 schweren kardialen Ereignissen und 138 Malignomen beendet werden konnte, um eine Power von 80 bzw. 90% zu erreichen, unter der angenommenen Ereignisrate von 1,0 und 1,1 pro 100 Patientenjahre (PJ). Bei der Fallzahlberechnung für die Studie wurde von ungefähr 4.000 Patient:innen, die rekrutiert werden müssen, ausgegangen, um diese Endpunkte zu erreichen, wenn mindestens 1.500 von ihnen 3 Jahre beobachtet werden würden.
Letztlich wurden 4.362 Patient:innen mit erhöhtem kardiovaskulären Risiko eingeschlossen, von denen 31 % mehr als 65 Jahre alt waren. Die Studie wurde 2020 nach Erreichen der Endpunkte abgeschlossen. Primärer Endpunkt war Nichtunterlegenheit von Tofacitinib gegenüber den TNFi in Hinblick auf schwere kardiovaskuläre Ereignisse (MACE) und Malignome (mit Ausnahme von Nicht-Melanom-Hautkrebs). Dabei wurde die obere Grenze des zweiseitigen Konfidenzintervalls (willkürlich) auf 1,8 festgesetzt für den Vergleich der kombinierten Tofacitinibgruppen vs. TNFi und auf 2,0 für den Vergleich der beiden Toficitinib-Dosierungen. Dieser Endpunkt wurde verfehlt, schwere kardiale Ereignisse traten unter Tofacitinib numerisch häufiger auf (der Unterschied war allerdings nicht signifikant). Für Malignome war die Inzidenzrate unter dem JAKi vs TNFi höher, aber auch nicht signifikant verschieden. Bei der höheren Wahrscheinlichkeit für Malignome unter Tofacitinib vs. TNFi war der Unterschied aber signifikant. Die Tabellen 1 und 2 zeigen die dazugehörigen Ergebnisse. Die darin enthaltenen Angaben zur "Number needed to harm" (NNH) zeigen die Seltenheit der entsprechenden Ereignisse: die NNH lag für schwere kardiale Ereignisse (MACE) für Tofacitinib in der Standarddosierung von 2 x 5 mg tgl. im Vergleich zu den TNFi bei 567, für 2x10 mg bei 319 pro PJ. In der Standarddosis legen die Daten daher ein einzelnes zusätzliches kardiovaskuläres Ereignis bei mehr als 550 mit Tofacitinib behandelten Patient:innen pro Jahr nahe. Bei den bösartigen Tumoren lag die NNH bei 276 für 2x5 mg tgl. und bei 275 für 2x10 mg pro PJ. Post-hoc-Analysen ergaben, dass dies vorwiegend bestimmte Risikogruppen betrafen. Hierzu zählten vor allem aktuelle und frühere Raucher, Alter über 65 Jahre, ein erhöhtes kardiales Risiko oder (anamnestisch) bekannte periphere arterielle Verschlusskrankheit. Eine speziell für die doppelte Dosis von 2x10 mg erhöht gefundene Rate für Gesamt-Mortalität und Lungenembolien führte dazu, dass Patient:innen aus dieser Dosisgruppe schon während der Studie in die 2x5 mg-Dosierung wechselten.
Bei der Interpretation der Daten zu den kardialen Ereignissen ist zu berücksichtigen, dass für TNFi in verschiedenen Untersuchungen ein protektiver kardiovaskulärer Effekt nachgewiesen wurde (8). Die numerische Unterlegenheit von Tofacitinib bedeutet also nicht zwangsläufig ein erhöhtes Risiko für MACE, sondern könnte auch durch einen weniger ausgeprägten protektiven Effekt im Vergleich zu TNFi bedingt sein. Um das zu verifizieren, hätte die Studie eine nur mit MTX behandelte Kontrollgruppe enthalten müssen. Zu den anderen Limitationen der Studie zählen neben dem selektiven Einschluss von Patient:innen mit Risikofaktoren, dem Fehlen weiterer Kontrollgruppen und der ungleich verteilten Verwendung der beiden TNFi, eine sehr hohe Rate an vorzeitigen Abbrüchen sowie eine (allerdings nur gering) erhöhte Rate an aktiven Raucher:innen in der Tofacitinib-Gruppe. Überdies sind schwere kardiale Ereignisse überwiegend in der nordamerikanischen Studienpopulation und erheblich weniger bei allen anderen Studienteilnehmern aufgetreten (9). Dies könnte damit zusammenhängen, dass vor allem in den USA viele Patient:innen mit hohem kardialem Risiko keine adäquate Therapie der Risikofaktoren erhalten haben, so erhielten z.B. nur ca. 50 % der Subgruppe mit einer anamnestisch bekannten arteriosklerotischen Herzerkrankung eine Statin-Therapie (10).
Unterdessen sind mehrere Post-hoc-Analysen aus der Studie publiziert. So konnte nachgewiesen werden, dass eine höhere Rate an MACE unter der Standarddosis Tofacitinib im Vergleich zu TNFi nur bei Patient:innen mit einer schon vorbekannten koronaren Herzerkrankung (KHK), nicht aber bei denen ohne diese Erkrankung zu finden war (10). Die NNH lag bei anamnestischer KHK bei 16, bei einer nicht vorbekannten KHK hingegen bei 869. In einer Nachanalyse der Malignom-Fälle zeigte sich hingegen, dass eine höhere Rate unter Tofacitinib im Vergleich zu TNFi erst allmählich zunehmend nach dem 18. Monat der Studie zu beobachten war, und dass das Risiko bei gleichzeitiger Anamnese einer KHK sowie bei hohem kardiovaskulärem Risikoscore höher war (11). Die Rate der Malignome war vorwiegend bei nordamerikanischen Patient:innen erhöht (11). Dort war auch der in anderen Studien mit Malignomen und erhöhten TNF-Spiegeln assoziierte BMI deutlich höher als in Europa.
In einer weiteren Nachanalyse, in der die Patient:innen in zwei Gruppen stratifiziert wurden - eine mit hohem Risiko (>65 Jahre oder aktive bzw. frühere Langzeitrauchende) und eine mit einem niedrigen Risiko (<65 Jahre, niemals geraucht) - wurde nur in der Hoch-Risiko-Gruppe unter der Exposition mit Tofacitinib ein erhöhtes Risiko für Malignome (außer Nicht-Melanom-Hautkrebs), MACE, Myokardinfarkt, Venenthrombosen und Gesamtmortalität festgestellt mit Hazard Ratios (HRs) von 1,41 bis 5,19 gegenüber TNFi. In der Gruppe mit einem niedrigen Risiko zeigte sich für Tofacitinib gegenüber TNFi für keines dieser Ereignisse ein signifikant erhöhtes Risiko (12).
Weitere Post-hoc-Analysen verglichen die Verträglichkeit von Tofacitinib und TNFi bei Erweiterung der ausgewerteten schweren kardialen Ereignisse (MACE) von drei auf acht Endpunkte (MACE 8). Neben Tod aus kardiovaskulärer Ursache, nicht tödlich verlaufenden Myokardinfarkten und Schlaganfällen wurden Hospitalisationen wegen instabiler Angina, koronarer Revaskularisation, transienter ischämischer Attacken, peripherer Vaskulopathie und Herzinsuffizienz berücksichtigt und zusätzlich venöse Thrombembolien (VTE) ausgewertet (13). MACE 8 boten in der HR keinen Unterschied zwischen den beiden Therapien, MACE 8+VTE nur für die höhere Tofacitinib-Dosierung von 2 x 10 mg. Bei RA-Dosierung bot Tofacitinib generell nur für Myokardinfarkte, nicht aber für die anderen KV-Ereignisse eine Risikoerhöhung. Bestehende arteriosklerotische Herzerkrankung und Alter > 65 Jahre waren risikosteigernde Faktoren.
Zudem wurde in einer Nachanalyse das Auftreten von VTE im Ablauf der Studie (in 6 Monats-Intervallen) erfasst und nach Risikofaktoren für VTE gesucht (14). Es bestätigte sich zunächst, dass nur für die Tofacitinib-Dosis 2 x 10 mg, aber nicht für die bei RA zugelassene Dosis 2 x 5 mg, eine erhöhte Rate im Vergleich zu TNFi feststellbar war. Im zeitlichen Verlauf der Studie zeigte sich eine konstante Rate an Ereignissen. Als Risikofaktoren waren positive Anamnese für VTE, ein BMI von > 35 kg/qm, höheres Lebensalter und die Anamnese einer chronischen Lungenerkrankung zu ermitteln.
Evidenz aus sonstigen Studien
Nur eine weitere Studie, die bei der Bewertung des Europäischen Pharmacovigilance Risk Assessment Committee (PRAC) auch mit hinzugezogen wurde, hat Hinweise für ein im Vergleich zu TNFi erhöhtes thrombembolisches und kardiovaskuläres Risiko unter JAKi-Therapie ergeben. In einer Studie, in der Therapiedaten aus 14 unterschiedlichen Real-World-Quellen (3 Register, 8 Krankenkassen) ausgewertet wurden (15), zeigte das Inzidenzratenverhältnis (IRR) thrombembolischer Ereignisse mit 1,51 (CI 1,10; 2,08) unter Baricitinib vs. TNFi ein höheres Risiko für VTE unter Baricitinib. In der Studie waren in 9 bzw. 10 Monaten 56 Fälle unter Baricitinib und 41 unter TNFi aufgetreten. MACE und schwere Infektionen waren numerisch, aber nicht signifikant, unter Baricitinib erhöht. Auch diese Studie hinterlässt offene Fragen. So sind die herangezogenen Datenquellen heterogen und lückenhaft. Ein Großteil der Daten entstammte zwei der 14 Quellen, dem schwedischen ARTIS- und dem französischen SNDS-Register. Bei SNDS war die Rate der MACE dreifach höher als bei ARTIS (Inzidenzrate/100 Patientenjahre 1,4 vs. 0,56), erklärbar möglicherweise durch eine überwiegende Erfassung schwerkranker Patient:innen mit fortgeschrittener Erkrankung. Die Krankheitsaktivität als wichtiger Einflussfaktor für Risiken wurde nicht erfasst.
Auswertungen aus dem RCT-Studienprogramm der vier JAKi haben - abgesehen vom Herpes zoster - generell keine Hinweise für eine Risikoerhöhung ergeben, wie sie in der ORAL SURVEILLANCE gefunden wurden. In einer Metaanalyse wurde auf der Basis von 29 ausgewerteten Studien eine Odds Ratio von 0,91 für das Risiko thrombembolischer Ereignisse unter JAKi ermittelt (16). Auswertungen aus dem gesamten Studienprogramm von Baricitinib (17), Upadacitinib (18, 19) und Filgotinib (20) ergaben ebenfalls keine Risikoerhöhungen für MACE, thrombembolische Ereignisse oder Malignome.
Auch einige weitere Auswertungen aus Registern konnten die in der ORAL-SURVEILLANCE-Studie gefundene Risikoerhöhung nicht bestätigen. Im deutschen RABBIT-Register wurden die MACE-Raten unter JAKi, TNFi und csDMARD im Zeitraum 2017 - 2022 verglichen (21). Weder in der RA-Gesamtpopulation noch in einer Subgruppe mit erhöhtem kardiovaskulärem Risiko war die Rate zwischen den drei Behandlungsarten unterschiedlich. Aus einer noch laufenden japanischen Post-Marketing-Surveillance-Studie wurden 24 Wochen-Daten von 4.731 RA-Patienten publiziert (22). Erhöht war erwartungsgemäß die Rate der Herpes zoster-Fälle (3,09 %), MACE traten nur in sieben Fällen (0,15 %), Malignome in 17 Fällen (0,36%) auf – beides entsprach der erwarteten Rate im RA-Krankengut. Das Risiko für das Auftreten von Malignomen wurde auch im dänischen DANBIO Register untersucht. Mit einer HR für Malignome von 1,4 (95% CI 0.75-2.37) für JAKi vs bDMARDs konnte kein signifikanter Unterschied festgestellt werden. Im schwedischen ARTIS-Register wurden schwere Nebenwirkungen bei mehr als 20.000 RA-Patient:innen ausgewertet (23). Auch hier fanden sich, abgesehen von der höheren Rate an Herpes zoster unter JAKi (Baricitinib und Tofacitinib), keine Unterschiede im Vergleich zu biologischen DMARDs (vorwiegend Etanercept) - insbesondere auch in Bezug auf MACE. Krankenkassendaten, die in der US-amerikanischen STAR-RA-Studie ausgewertet wurden, zeigten ein numerisch, aber nicht signifikant erhöhtes MACE-Risiko unter Tofacitinib im Vergleich zu TNFi in der nach den ORAL-Surveillance Einschlusskriterien ausgewählten Patient:innengruppe, nicht aber in der unselektierten „real-world“ Kohorte (24). Im CorEvitas-Register aus den USA waren die 5-Jahres-Inzidenzraten für MACE vergleichbar unter Therapie mit Tofacitinib und anderen biologischen DMARDs (25). Das spezifische Risiko für thrombembolische Ereignisse unter Tofacitinib im Vergleich zu TNFi wurde in einer weiteren Auswertung der auch in der Star RA Studie inkludierten Krankenkassendaten bei 87.653 RA-Patienten untersucht (26). Thrombembolische Ereignisse waren auch hier generell selten und gleich häufig unter Tofacitinib und TNFi.
In der sogenannten JAK-pot Studie (27) wurde die nebenwirkungsbedingte Beendigung von RA-Therapien mit Zweitlinien-DMARDs aus 17 Registern ausgewertet. Der Vergleich von JAKi, TNFi und bDMARDs mit anderen Wirkmechanismen ergab vergleichbare Abbruchraten zwischen JAKi und TNFi, wobei die Behandlung mit Tofacitinib häufiger, die mit Baricitinib seltener als die mit TNFi beendet wurde. Vergleicht man nur Patient:innen, die älter als 65 Jahre waren oder einschlägige kardiovaskuläre Risikofaktoren aufwiesen, ist die Abbruchrate aufgrund von Nebenwirkungen unter JAKi höher als unter TNFi.
Insgesamt deuten die Daten zunehmend darauf hin, dass das Risiko für MACE, venöse Thrombembolien und Malignome unter JAKi-Therapie stark vom Vorhandensein entsprechender Risikofaktoren abhängt. Wenn diese nicht vorliegen, ergibt sich offenbar kein erhöhtes Risiko für die genannten Ereignisse im Vergleich zu TNFi. Insbesondere im Hinblick auf kardiovaskuläre Ereignisse und Thrombembolien ist gut belegt, dass neben der guten, glukokortikoidfreien Kontrolle der Krankheitsaktivität der Einsatz von TNFi das Risiko signifikant senkt und TNFi in diesen Situationen präferiert werden sollten.
Aus den EMA-Empfehlungen resultierende Einschränkungen für die Anwendung von JAK-Inhibitoren
Die EMA hat die nur mit Tofacitinib bei RA erarbeiteten Daten der ORAL- SURVEILLANCE-Studie im Analogieschluss auf die anderen drei JAKi sowie auf alle mit JAKi behandelten Erkrankungen übertragen, auch wenn konkrete Daten hierzu bisher nicht existieren (28). Diese Risiken betreffen kardiovaskuläre Erkrankungen, Thrombosen, Malignome und Infektionen. Daraufhin wurden die Fachinformationen zu den vier in der Rheumatologie eingesetzten JAKi Baricitinib, Filgotinib, Tofacitinib und Upadacitinib entsprechend aktualisiert.
Patient:innen mit spezifischen Risiken für die o.g. Nebenwirkungen sollten demnach nur dann mit JAKi behandelt werden, wenn keine geeignete Therapiealternative zur Verfügung steht. Zudem sollte bei Risikopatient:innen versucht werden, im Falle einer Therapie mit JAKi deren Dosis wenn möglich zu reduzieren.
Die o.g. Risiken betreffen:
-
Patient:innen ab dem 65. Lebensjahr
-
Patient:innen mit erhöhtem Risiko für schwere kardiovaskuläre Komplikationen, d.h. mit bereits durchgemachtem Herzinfarkt, ischämischem Schlaganfall oder bekannter peripherer arterieller Verschlusskrankheit sowie auch solche mit bekannter, klinisch bedeutsamer Arteriosklerose
-
Patient:innen, die rauchen oder früher längere Zeit geraucht haben
-
Patient:innen mit erhöhtem Malignomrisiko auch über das Rauchen hinaus. Dies betrifft in erster Linie Patient:innen mit bekannter bzw. behandelter maligner Erkrankung sowie Patient:innen mit besonderen Risiken für eine maligne Erkrankung wie z. B. ererbte Risiken oder besondere Exposition gegenüber Kanzerogenen
Darüber hinaus wird empfohlen, JAKi mit besonderer Vorsicht einzusetzen bei Patient:innen mit erhöhtem Risiko für venöse thrombembolische Erkrankungen, die nicht zu den o.g. Risikogruppen gehören. Hierunter fallen zunächst solche Patient:innen, die bereits eine venöse Thrombose oder eine Lungenembolie erlitten haben, insbesondere wenn sie nicht mehr antikoaguliert sind. Zudem ist die Indikation zum Einsatz von JAKi bei Patient:innen mit angeborenen Thrombophilien oder in Phasen von krankheits- oder therapieassoziiertem erhöhten Thrombembolierisiko besonders streng zu stellen.
Einschätzung des kardiovaskulären und Tumor-Risikos
Nach den vorliegenden Daten und EMA-Empfehlungen stellt sich die Frage, welche Patient:innen zu den o.g. Risikogruppen gehören.
Ein erhöhtes kardiovaskuläres Nebenwirkungsrisiko besteht bei schon bekannter kardiovaskulärer Erkrankung, d.h. nach kardiovaskulärem Ereignis oder bei nachgewiesener relevanter Arteriosklerose. Behandelte und gut eingestellte Risikofaktoren wie Diabetes mellitus oder arterielle Hypertonie zeigen für sich genommen jedoch keine Risikoerhöhung für MACE unter JAKi. Für eine substanzielle Risikoreduzierung durch adäquate Behandlung dieser "traditionellen" Risikofaktoren gibt es einerseits hohe Evidenz (29, 30, 31). Andererseits war die Behandlung dieser Risikofaktoren in der Hochrisikopopulation der ORAL SURVEILLANCE Studie offenbar stark defizitär (10).
Aktive Raucher gehören ebenfalls zur Risikogruppe, wobei das Risiko mit der Zahl gerauchter Zigaretten pro Tag, der Dauer des Rauchens bzw. mit der kumulativen Dosis steigt (33). Bei Ex-Raucher:innen nimmt das kardiovaskuläre Risiko schon 2 Jahre nach Beendigung des Rauchens signifikant ab und gleicht nach 5 bis spätestens 10 Jahren dem von Nichtraucher:innen (34, 35).
Das Lungenkrebsrisiko (und das Risiko für viele andere Malignome) ist bei Raucher:innen ebenfalls dosisabhängig erhöht (36). Wird das Rauchen aufgegeben, nimmt das Risiko schon nach 5 Jahren messbar ab, um nach 15 bis 20 Jahren das von Personen, die niemals geraucht hatten, zu erreichen (37).
Alter > 65 als Risikofaktor?
Die generelle Einstufung des Alters ab 65 Jahre als Risikofaktor durch die EMA ist kritisch zu hinterfragen. Tatsächlich wurde dieser Risikofaktor ausschließlich in der ORAL SURVEILLANCE-Studie ermittelt. Das bedeutet, dass ausschließlich Patient:innen > 65 mit hohem kardiovaskulärem Risiko (Einschlusskriterium der Studie!) diese Risikoerhöhung boten. Bisher gibt es keine Studie, die belegen würde, dass Patient:innen > 65 ohne hohes kardiovaskuläres Risiko durch Einnahme von JAKi vermehrt gefährdet wären. Im Gegenteil: In einer Kohortenstudie aus dem schwedischen Rheumatology Quality Register, die den Zeitraum 2016 - 2021 und 13.492 RA-Patienten umfasste, wurde weder in der Gesamtanalyse noch in der Subpopulation mit Alter > 65 ein Unterschied in der Rate schwerer kardiovaskulärer Ereignisse unter JAKi, TNFi und bDMARD mit anderem Wirkmechanismus gefunden (38). Im zweiten Teil der Untersuchung wurde der Nutzen dieser Therapien analysiert (39). Hier erwies sich, dass Patient:innen > 65 besonders von der Therapie mit JAKi profitierten, die Response-Rate lag deutlich über der unter TNFi und non-TNF-bDMARD.
Was ist vor der Neuverordnung eines JAKi zu tun?
Hinweise zu möglichen besonderen Risiken einer JAKi-Therapie stellen keine Zulassungsbeschränkungen oder Kontraindikationen dar, sondern geben Empfehlungen zur Erhöhung der Therapiesicherheit von JAKi. D.h. bei jeder zulassungs- und leitliniengemäßen Behandlung mit einem JAKi, muss unter Berücksichtigung der aktuellen Empfehlungen das individuelle Nebenwirkungsrisiko beurteilt, gegen den zu erwartenden Nutzen abgewogen und schließlich mit der Patientin oder dem Patienten gemeinsam eine Therapieentscheidung getroffen werden.
Nach Prüfung der Indikation und Ausschluss von Kontraindikationen müssen vor Einleitung einer Therapie mit JAKi zusätzlich folgende Risiken für schwerwiegende Nebenwirkungen berücksichtigt werden:
-
Alter: > 65 Jahre (Anmerkung siehe oben)
-
hohes kardiovaskuläres Risiko: bekannte koronare Herzerkrankung, signifikante Arteriosklerose (z. B. periphere arterielle Verschlusskrankheit), früheres kardiovaskuläres Ereignis (z. B. Myokardinfarkt, ischämischer Schlaganfall)
-
hohes thrombembolisches Risiko: frühere venöse Thrombose oder Lungenembolie, bekannte Thrombophilie (z.B. Prothrombin-Mutation, Faktor V-Leiden-Mutation, …), aktuelle Erkrankungen oder Medikation, die mit einem erhöhten Thromboserisiko einhergehen
-
Raucherstatus: aktiver Raucher oder Ex-Raucher (seit wann, siehe Text)
-
Tumorrisiko: besteht oder bestand eine maligne Erkrankung, ist ein erhöhtes Tumorrisiko bekannt (familiär, Exposition)
Sollte ein besonderes Nebenwirkungsrisiko identifiziert werden, sollte der JAKi nur verordnet werden, wenn in der individuellen Situation keine geeignete, also mindestens vergleichbar wirksame und mit einem geringeren Nebenwirkungsrisiko behaftete Therapiealternative besteht. Das bedeutet ausdrücklich nicht, dass zuvor alle zur Behandlung der Erkrankung zugelassenen DMARDs eingesetzt werden müssen, sondern dass eine sorgfältige, individuelle Nutzen-/Risikoabwägung getroffen, mit den Patient:innen besprochen und dokumentiert wurde. Dabei ist immer auch die zu erwartende Wirksamkeit der in Frage kommenden Medikamente zu berücksichtigen. Eine schlecht eingestellte entzündlich-rheumatische Erkrankung ist meist mit einem höheren Risiko verbunden als der Einsatz von JAKi mit Erreichen einer Remission.
Was ist bei bereits laufender Therapie mit JAKi zu tun?
Bei Patient:innen mit gut laufender JAKi-Therapie stellt die Abwägung zwischen der möglichen Risikoerhöhung durch die JAKi und dem Risiko einer Therapieumstellung eine besondere Herausforderung dar. Auch bei diesen Patient:innen sollte eine Risikoevaluation nach o.g. Liste erfolgen. Wenn danach ein besonderes Risiko für eine schwerwiegende Nebenwirkung identifiziert wurde, sollte der Patient/ die Patientin hierüber informiert und die Fortsetzung oder Umstellung der Therapie unter erneuter Nutzen-Risikoabwägung besprochen werden.
Eine sorgfältige Dokumentation der Erfassung von Nebenwirkungsrisiken und der mit dem Patienten gemeinsam getroffenen Therapieentscheidung, z. B. anhand einer Checkliste und der DGRh-Therapieinformationsbögen, wird angeraten.
Anmerkung
Inwieweit die auf der Basis der Ergebnisse der ORAL SURVEILLANCE-Studie ermittelten Risiken tatsächlich auf die Anwendung der JAKi außerhalb dieser Studie übertragbar sind, bleibt weiterhin unklar. Sicher ist hingegen anhand zahlreicher Untersuchungen, dass die unbehandelte bzw. unzureichend behandelte RA mit einem massiv erhöhten Risiko für kardiovaskuläre (40) und thrombembolische Komplikationen (41) sowie mit einem erhöhten Risiko für das Auftreten von Lymphomen (42) und weiteren Malignomen (43) verbunden ist. Ebenso erhöht die Behandlung mit dauerhaft höheren Dosen von Glukokortikoiden das Risiko für kardiovaskuläre und thrombembolische Komplikationen deutlich (44, 45). Bestmögliche Kontrolle der Krankheitsaktivität durch DMARDs und die Verfolgung des Therapieziels Remission unter Vermeidung alternativer Therapien mit hohen Risiken muss deshalb bei der Behandlung oberste Priorität haben. Vermutete, aber nicht sicher belegte Risiken sollten nicht dazu führen, dass auf den Einsatz eines hochwirksamen Therapieprinzips, wie es die JAKi darstellen, verzichtet wird, wenn aus dem Verzicht eine schlechtere Krankheitskontrolle oder der vermehrte Einsatz von Glukokortikoiden resultiert.
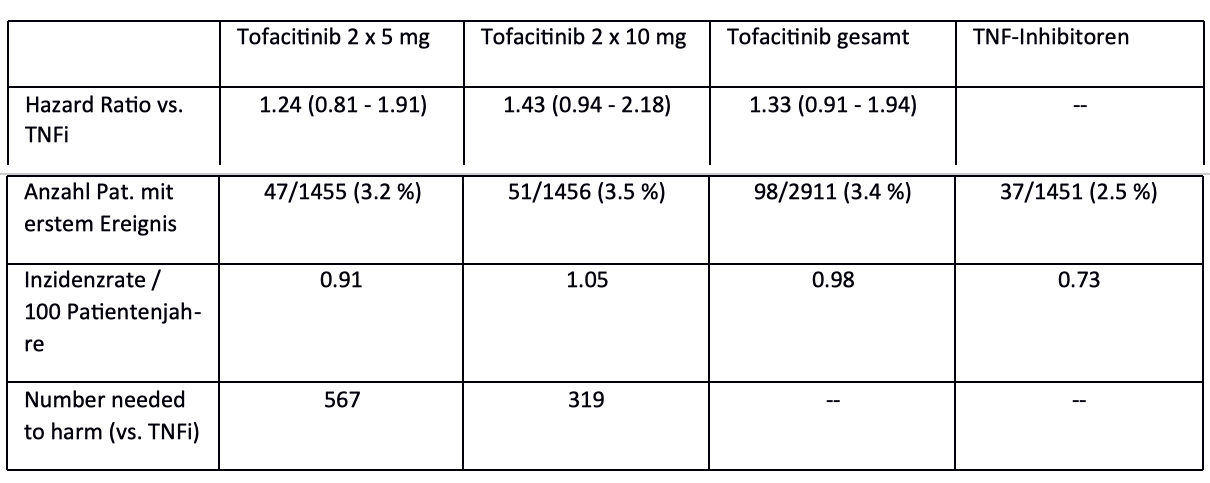
Tabelle 1: Hazard Ratio und Inzidenzrate für bestätigte schwere kardiale Ereignisse (nach 6)
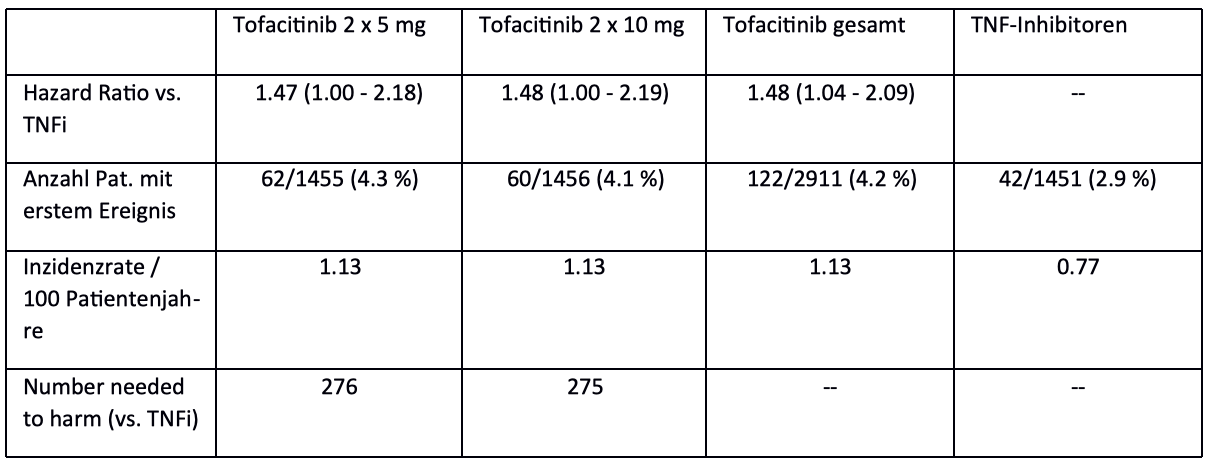
Tabelle 2: Hazard Ratio und Inzidenzrate für Malignome (exkl. Non-Melanom-Hautcarcinom) (nach 6)
Das Wichtigste in Kürze
Seit Erscheinen der Warnhinweise für die Anwendung von JAK-Inhibitoren (JAKi) durch die EMA Anfang 2023 und der Empfehlungen der DGRh zu diesem Thema vor mehr als einem Jahr sind hierzu eine Reihe neuer Publikationen erschienen, die eine Überarbeitung erforderlich machten. Nachfolgend sind die wichtigsten Neubewertungen der Evidenz zum Einsatz von JAKi kurz zusammengefasst:
1) Alter über 65 Jahre: Evidenz für ein erhöhtes Risiko dieser Altersgruppe bei Therapie mit JAKi im Vergleich zu anderen DMARD gibt es nur bei gleichzeitigem Vorliegen eines hohen kardiovaskulären Risikos, nicht aber für Patienten ohne dieses zusätzliche Risiko.
2) Ein hohes kardiovaskuläres Risiko liegt bei bekannter koronarer Herzerkrankung, signifikanter Arteriosklerose und anamnestischen kardiovaskulären Ereignissen (Herzinfarkt, Schlaganfall) vor, aber nicht bei alleinigem Vorliegen gut behandelter Risikofaktoren wie Hypertonie oder Diabetes mellitus.
3) Aktives Rauchen und früheres Rauchen innerhalb der letzten 20 Jahre zählen weiter zu den Risikofaktoren; exaktere Angaben zu Menge und Zeitraum sind aufgrund der Datenlage nicht möglich.
4) Bei erhöhtem Malignom-Risiko (vor allem Malignome in der Anamnese) ist der Einsatz von JAKi nur bei Fehlen gleichwertiger Alternativen zu empfehlen.
5) Dies gilt ebenso bei hohem thrombembolischem Risiko (insbesondere positiver Anamnese, bekannter Thrombophilie).
Nach wie vor gilt: Warnhinweise sind nicht identisch mit Kontraindikationen, sondern sollten bei Vorliegen Anlass für eine individuelle Nutzen-Risiko-Abwägung sein. Die Therapie-Entscheidung sollte gemeinsam mit dem Patienten (nach Aufklärung) getroffen und dokumentiert werden. Die bestmögliche Kontrolle der Krankheitsaktivität sollte dabei hohe Priorität haben.
Autoren:
Für die Deutsche Gesellschaft für Rheumatologie und Klinische Immunologie:
Prof. Dr. Andreas Krause, für den Vorstand der DGRh
Prof. Dr. Klaus Krüger, für die Kommission Pharmakotherapie der DGRh
Literatur
1. Thiele K, Albrecht K, Kopplin N, Callhoff J. Deutsches Rheuma-Forschungszentrum (DRFZ) Berlin, Programmbereich Epidemiologie und Versorgungsforschung. Standardpräsentation 2021, Daten aus der Kerndokumentation. https://www.drfz.de/wp-content/uploads/ergebnisse-kerndokumentation-2021.pdf, abgerufen am 13.03.20232.
2. Taylor PC, Keystone EC, van der Heijde D, et al. (2017) Baricitinib versus placebo or adalimumab in rheumatoid arthritis. N Engl J Med. 376: 652–662.
3. Fleischmann R, Pangan AL, Song IH et al. (2019) Upadacitinib versus Placebo or Adalimumab in Patients with Rheumatoid Arthritis and an Inadequate Response to Methotrexate: Results of Phase 3, Double-Blind, Randomized Controlled Trial. Arthritis Rheum 71: 1788 - 1800.
4. Combe B, Kivitz A, Tanaka Y et al. (2021) Filgotinib versus placebo or adalimumab in patients with rheumatoid arthritis and inadequate response to methotrexate: a phase III randomised clinical trial. Ann Rheum Dis 80: 848 - 858.
5. Rubbert-Roth A, Enejosa J, Pangan AL et al (2020) Trial of Upadacitinib or Abatacept in Rheumatoid Arthritis. N Engl J Med 383: 1511 - 1521.
6. Van de Laar M, Voshaar MO, ten Klooster P et al. (2023) Baricitinib versus TNF-inhibitors in Patients with Active Rheumatoid Arthritis After Failure of CsDMARDs: A Pragmatic, Multicenter, Real-Life Study in a Treat-to-Target Setting. Arthritis Rheum 75; 59 (Suppl.1) 872 - 874.
7. Ytterberg SR, Bhatt DL, Mikuls TR et al. (2022) Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med 386: 316 - 326.
8. Barnabe C, Martin B-J, Ghali WA. (2011) Systematic review and meta-analysis: antitumor necrosis factor α therapy and cardiovascular events in rheumatoid arthritis. Arthritis Care Res 63: 522-529.
9. Szekanecz Z,, Giles JT, Buch MH et al. Incidence of major adverse cardiovascular events stratified by geographic region and baseline cardiovascular risk: A post-hoc analysis of ORAL SURVEILLANCE. Ann Rheum Dis 2022; 10.1136/annrheumdis-2022-eular.1180
10. Charles-Schoeman C, Buch MH, Dougados M et al. (2023) Risk of major adverse cardiovascular events with tofacitinib versus tumour necrosis factor inhibitors in patients with rheumatoid arthritis with or without a history of atherosclerotic cardiovascular disease: a post hoc analysis from ORAL Surveillance. Ann Rheum Dis 82: 119 - 129.
11. Curtis JR, Yamaoka K, Chen YH et al. (2023) Malignancy risk with tofacitinib versus TNF inhibitors in rheumatoid arthritis: results from the open-label, randomised controlled ORAL Surveillance trial. Ann Rheum Dis 82: 331 - 343.
12. Kristensen LE, Danese S, Yndestad A, Wang C, Nagy E, Modesto I, Rivas J, Benda B (2023). Identification of two tofacitinib subpopulations with different relative risk versus TNF inhibitors: an analysis of the open label, randomised controlled study ORAL Surveillance. Ann Rheum Dis. 82(7):901-910. Erratum in: Ann Rheum Dis. 2024 Feb 15;83(3):e11. doi: 10.1136/ard-2022-223715corr1
13. Buch MH, Bhatt DL, Charles-Schoeman C et al. Risk of extended major adverse cardiovascular event endpoints with tofacitinib versus TNF inhibitors in patients with rheumatoid arthritis: a post hoc analysis of a phase 3b/4 randomised safety study. RMD Open 2024; 10: e003912
14. Charles-Schoeman C, Fleischmann R, Mysler E et al. Risk of Venous Thromboembolism With Tofacitinib Versus Tumor Necrosis Factor Inhibitors in Cardiovascular Risk-Enriched Rheumatoid Arthritis Patients. Arthritis Rheum 2024; Mar 13, doi: 10.1002/art.42846.
15. Salinas CA, Louder A, Polinski J et al. (2023) Evaluation of VTE, MACE, and Serious Infections Among Patients with RA Treated with Baricitinib Compared to TNFi: A Multi-Database Study of Patients in Routine Care Using Disease Registries and Claims Databases. Rheumatol Ther 10: 201 - 223.
16. Bilai J, Riaz IB, Naqvi SAA et al. (2021) Janus Kinase Inhibitors and Risk of Venous Thromoembolism: A Systematic Review and Metaanalysis. Mayo Clin Proc. 96: 1861 - 1873.
17. Taylor PC, Takeuchi T, Burmester GR et al (2022) Safety of baricitinib for the treatment of rheumatoid arthritis over a median of 4.6 and up to 9.3 years of treatment: final results from long-term extension study and integrated database. Ann Rheum Dis 81: 335 - 343.
18. Charles-Schoeman C, Choy E, McInnes IB et. al. (2022) MACE and VTE Across Upadacitinib Clinical Trial Programs in Rheumatoid Arthritis, Psoriatic Arthritis, and Ankylosing Spondylitis. Arthritis Rheum 74; S9: 1016 - 1019 (Abstr. 0510).
19. Rubbert-Roth A, Kakehasi A, Takeuchi T et. al. (2022) Malignancy in the Upadacitinib Clinical Trial Programs for Rheumatoid Arthritis, Psoriatic Arthritis, and Ankylosing Spondylitis. Arthritis Rheum 74; S9: 562 - 564 (Abstr. 0292).
20. Winthrop KL, Tanaka Y, Takeuchi T et al. (2022) Integrated safety analysis of filgotinib in patients with moderately to severely active rheumatoid arthritis receiving treatment over a median of 1.6 years. Ann Rheum Dis 81: 184 - 192.
21. Meissner Y, Schäfer M, Albrecht K et al. (2023) Risk of major adverse cardiovascular events in patients with rheumatoid arthritis treated with conventional synthetic, biologic and targeted synthetic disease-modifying antirheumatic drugs: observational data from the German RABBIT register. RMD Open 2023; 9: e003489.
22. Takagi M, Atsumi T, Matsuno H et al. (2022) Safety and Effectiveness of Baricitinib for Rheumatoid Arthritis in Japanese Clinical Practice: 24-Week Results of All-Case Post-Marketing Surveillance. Mod Rheumatol. Aug 6;roac089.doi: 10.1093/mr/roac089.
23. Frisell T, Bower H, Morin M et al. (2023) Safety of biological and targeted synthetic disease-modifying antirheumatic drugs for rheumatoid arthritis as used in clinical practice: results from the ARTIS programme. Ann Rheum Dis online Feb 14; 10.1136/ard-2022-223762.
24. Khosrow-Khavar F, Kim SC, Lee H, et al. (2022) Tofacitinib and risk of cardiovascular outcomes: results from the Safety of Tofacitinib in Routine care patients with Rheumatoid Arthritis (STAR-RA) study. Ann Rheum Dis 81:798-804.
25. Kremer JM, Bingham CO, 3rd, Cappelli LC, et al. (2021) Postapproval Comparative Safety Study of Tofacitinib and Biological Disease-Modifying Antirheumatic Drugs: 5-Year Results from a United States-Based Rheumatoid Arthritis Registry. ACR Open Rheumatol 3:173-184.
26. Desai RJ, Pawar A, Khosrow-Khavar F et al. (2022) Risk of venous thromboembolism associated with tofacitinib in patients with rheumatoid arthritis: a population-based cohort study. Rheumatology 61: 121 - 130.
27. Aymon R, Mongin D, Bergstra SA, et al. (2023) Evaluation of discontinuation for adverse events of JAK inhibitors and bDMARDs in an international collaboration of rheumatoid arthritis registers (the `JAK-pot` study). Ann Rheum Dis 2023 Dec 8. Doi:10.1136/ard-2023-224670
28. European Medicine Agency. Januskinase Inhibitors. https://www.ema.europa.eu/en/medicines/human/referrals/janus-kinase-inhibitors-jaki2023, abgerufen am 13. März 2023.
29. Navarese EP, Robinson JG, Kowalewski M et al. Association Between Baseline LDL-C Level and Total and Cardiovascular Mortality After LDL-C Lowering: A Systematic Review and Meta-analysis. JAMA 2018; 319: 1566 - 1579.
30. Shi Q, Nong K, Vanvik PO et al. Benefits and harms of drug treatment for type 2 diabetes: systematic review and network meta-analysis of randomised controlled trials. BMJ 2023; 381: e074068.
31 Ettehad D, Emdin CA, Kiran A et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet 2016; 387: 957 - 967.
33. Dunn NR, Faragher B, Thorogood M, et al. (1999) Risk of myocardial infarction in young female smokers. Heart 82:581-583
34. Wolf PA, D'Agostino RB, Kannel WB, Bonita R, Belanger (1988). Cigarette smoking as a risk factor for stroke. The Framingham study. JAMA 259:1025-1029
35. Ohsawa M, Tanno K, Ogasawara K, et al. (2019) The Absolute Risk of Death and Cardiovascular Diseases in Past Smokers With a 10-year Cessation is Identical to the Risk in Never Smokers. Circulation 140.Suppl. 1: A12059
36. Tsoi KK, Pau YY, Wu WK, Chan FKL, Griffiths SM, Sung JJ (2009). Cigarette smoking and the risk of colorectal cancer: A meta-analysis of prospective cohort studies. Gastroenterology, suppl. 1 136:A614-A615
37. Meza R, Hazelton WD, Colditz GA, Moolgavkar SH (2008) Analysis of lung cancer incidence in the nurses' health and the health professionals' follow-up studies using a multistage carcinogenesis model. Cancer Causes Control 19:317-328
38. Bower H, Frisell T, di Giuseppe D et al. Comparative cardiovascular safety with janus kinase inhibitors and biological disease-modifying antirheumatic drugs as used in clinical practice: an observational cohort study from Sweden in patients with rheumatoid arthritis. RMD Open 2023; 9: e003630.
39. Bower H, Frisell T, di Giuseppe D et al. Are JAKis more effective among elderly patients with RA, smokers and those with higher cardiovascular risk? A comparative effectiveness study of b/ tsDMARDs in Sweden. RMD Open 2023; 9: e003648.
40. England BR, Thiele GM, Anderson DR, Mikuls TR (2018) Increased cardiovascular risk in rheumatoid arthritis: mechanisms and implications. BMJ 361:k1036. doi: 10.1136/bmj.k1036.
41. Molander V, Bower H, Frisell T, Askling J (2021) Risk of venous thromboembolism in rheumatoid arthritis, and its association with disease activity: a nationwide cohort study from Sweden. Ann Rheum Dis 80: 169 - 175.
42. Askling J, Fored CM, Baecklund E et al. (2005) Haematopoietic malignancies in rheumatoid arthritis: lymphoma risk and characteristics after exposure to tumour necrosis factor antagonists. Ann Rheum Dis 64: 1414 - 1420.
43. Simon TA, Thompson A, Gandhi KK et al. (2015) Incidence of malignancy in adult patients with rheumatoid arthritis: a meta-analysis. Arthritis Res Ther 2015; 17: 212.
44. Ocon AJ , Reed G , Pappas DA , et al . Short-term dose and duration-dependent glucocorticoid risk for cardiovascular events in glucocorticoid-naive patients with rheumatoid arthritis. Ann Rheum Dis 80:1522–1529.
45. Yoshimura M, Fujieda Y, Sugawara M et al. (2022) Disease activity as a risk factor for venous thromboembolism in rheumatoid arthritis analysed using time-averaged DAS28CRP: a nested case-control study. Rheumatol Int. 42:1939-1946
Stand: 17.10.2024
